شیمی تجزیه یک با کیفیت و کمیت
کمّیَت یا چَندی در لغت به معنای مقدار می باشد و معمولاً در برابر واژهٔ کیفیت به کار می رود
کمیت:
کمیت را می توان با یک عدد نشان داد و برای تعیین این مقدار نیاز به واحد (یکا) آن کمیت داریم
هرچیز که قابل اندازه گیری باشد.(زمان،طول،جرم،مساحت،سرعت...)
.لینک دانلود و خرید پایین توضیحات
دسته بندی : پاورپوینت
نوع فایل : .pptx ( قابل ویرایش و آماده پرینت )
تعداد اسلاید : 247 اسلاید
شیمی تجزیه یک
شیمی تجزیه با تعیین کیفی و کمی مواد
سرو کار دارد
تجزیه کیفی تعیین هویت یک گونه شمیایی
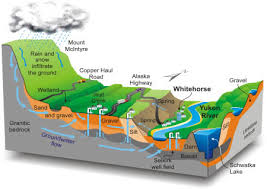
مثلا اگر یک آلوده کننده در یک رودخانه ماهیها را از بین می برد تجزیه کیفی را می توان برای تعیین هویت شیمیایی این آلوده کننده بکار برد
تجزیه کمی تعیین غلظت یک گونه شیمیایی مشخص
تعیین غلظت جیوه در یک رودخانه آلوده
تقسیم بندی روش کار یک تجزیه شیمیایی
روش کار کلاسیک (تر)
روش کار دستگاهی
برخی از روشهای نوری
تجزیه با اشعه x
تجزیه در ناحیه مرئی- ماورا بنفش
تجزیه ناحیه مرئی
تجزیه ناحیه IR
تجزیه ناحیه امواج رادیویی
تعادل شیمیایی
اگر دو واکنش دهنده a و b باهم مخلوط شوند
یک واکنش شیمیایی می تواند روی دهد و محصولات واکنش C و D را تولید کند
aA + bB cC + dD
در بسیاری از واکنشهای شیمیایی واکنش عکس
یعنی واکنش C با D برای تشکیل A و B نیز ممکن است
aA + bB = cC+dD
وقتی واکنش به ظاهر متوقف می شود
سیستم به تعادل شیمیایی می رسد در آن صورت
Keq = acC adD
aaA abB
در اینجا Keq ثابت تعادل نامیده می شود .
a فعالیت است که به صورت زیر با غلظت ارتباط دارد
a = fc
اگر غلظت جایگزین فعالیت شود
Keq = [C]c [D]d
[A]a [B]b
مولاریته
یک واحد غلظت است ، تعداد مولهای یک ماده
در یک لیتر (مول در لیتر)
مولاریته یک محلول با تقسیم تعداد مولهای ماده موجود در محلول بر حجم محلول بر حسب لیتر تعیین می شود.
معرفی برخی انواع ثابت تعادل :
تفکیک خودبه خودی آب
ثابت اسیدی
ثابت تعادل بازی
ثابت تشکیل کمپلکس
ثابت انحلال پذیری
تمرین 2-2. غلظت استات را در یک محلول آبی 0.10M استیک اسیدی محاسبه کنید . Ka = 1.8 x 10-5
HC2H3O2 = H+ + C2H3O2-
Ka = [H+][C2H3O2-] = 1.8 x 10-5
[HC2H3O2 ]
اگر از تفکیک خودبخودی آب صرف نظر کنیم
[H+] = [C2H3O2-]
1.8 x 10-5 = [C2H3O2-]2
0.10 - [C2H3O2-]